cDTIの概要
心機能と心筋の微細構造は密接に関連しており、微細構造の乱れは心筋疾患の病態に重要なことが分かってきました。
心臓拡散テンソルイメージング(cardiac Diffusion Tensor Imaging: cDTI)は、心筋の微細構造を非侵襲的に可視化・定量化できる技術です。この技術は、組織内の水分子が熱エネルギーによってランダムに移動する「ブラウン運動」を利用し、造影剤を使用しません。
心筋内では、細胞膜や細胞内構造が障壁となるため、水分子は心筋繊維の長軸方向に沿って拡散しやすくなります。cDTIは拡散の「方向性」と「強さ」を測定することで、組織の微細構造を推定し、下記のような定量値をもって評価することが可能です。
- Mean diffusivity (MD) と Fractional anisotropy (FA)
MDは拡散の全体的な強さを、FAは拡散がいかに一方向に揃っているかを示します。これらは、心筋の線維化や細胞配列の不規則性(錯乱)を反映します。 - Helix angle (HA)
心筋細胞は、心外膜側から心内膜側にかけて、その走行角度が連続的に変化する螺旋(ヘリックス)状の構造を持っています。HAはこの心筋細胞の傾きを定量化する指標です。 - Transverse angle (TA)
心筋細胞が心外膜の接線平面から心室腔(内側)に向かってどれだけ傾いているかを示す指標です。HAに比べ値は非常に小さいですが、細胞が壁の面から内側へ入り込む角度を定量化します。 - Sheetlet angle (E2A)
心筋細胞は、厚さ4〜6個分ほどの細胞が層状に重なった「シートレット」と呼ばれる構造を形成しています。このシートレット間の隙間がスライドすることで、心筋は収縮時に厚みを増すことができます。E2Aはこの層の傾きを測定し、収縮期と拡張期の可動性(E2A mobility)も評価することが可能です。
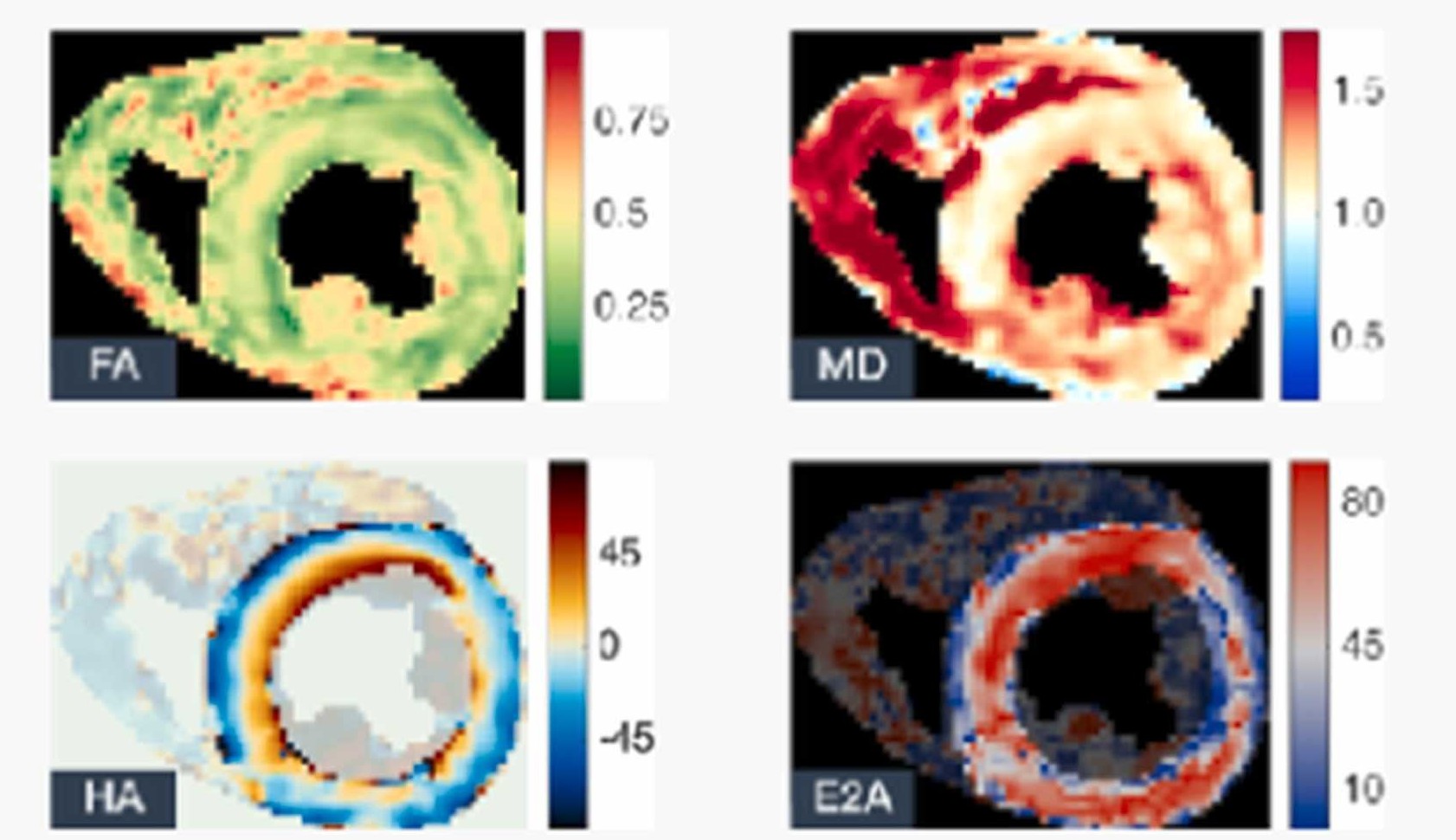
Fig.1 健常者の各種マップ画像(参考文献1.より引用)
cDTIは、非侵襲的な心筋性状評価、早期診断への寄与、予後予測とリスク層別化などが期待されています。
- 非侵襲的な心筋性状評価
心筋生検に比較し、より広範を非侵襲的に評価したり、造影検査に代わる手法として期待されています。
心筋生検との比較:心筋生検は特定の部位のみを採取・評価するのに対し、cDTIは非侵襲的に撮像領域全体を包括的に評価することができます。
造影検査との比較:特に腎機能障害を持つ患者に対して、造影検査(LGE)に代わる評価手法として期待されています。2) - 早期診断への寄与
cDTI指標の変化は、組織構造の変化や微小血管障害の初期兆候と関連する可能性が示唆されており、疾患の早期マーカーとなる可能性が期待されています。
早期表現型のバイオマーカー:心筋肥大が顕在化する前の組織学的な心筋細胞の錯乱や心筋灌流異常を捉えられるなど、マクロな形態変化が起こる前の「早期表現型」のバイオマーカーとして有用であると報告されています。3)4) - 予後予測とリスク層別化
心筋の微細構造の乱れを定量化することで、従来の指標よりも早期かつ高精度に将来の心機能不全や突然死リスク等を予測できることが期待されています。
心筋梗塞後のリモデリング予測: 急性期の梗塞部位における低いFA値や低い収縮期E2Aは、12か月後の左室悪性リモデリングの独立した予測因子となる可能性が報告されています。5)
突然死リスクの評価: HCM患者の心筋肥大部位における拡張期FAの低下は、NSVT(非持続性心室頻拍)の発生と独立して相関しており、突然死のリスク層別化に寄与する新たな指標として期待されています。6)
2.cDTIの撮像・パラメータ・解析について
cDTIは、心電図同期と呼吸同期(もしくは息止め)を併用する撮像です。心拍や呼吸状況によりますが、同期の場合約5~10分程度で撮像が可能です。cDTIを撮像することで、下図のようにλ1~λ3、e1~e3の値が得られ、λ1~λ3を元にFA,MDの値, e1を元にHA、TAの値、e2を元にE2Aの値を得ることができます。1)
HA、TA、E2Aは局所心臓座標系を使って算出する、cDTI特有の値です。
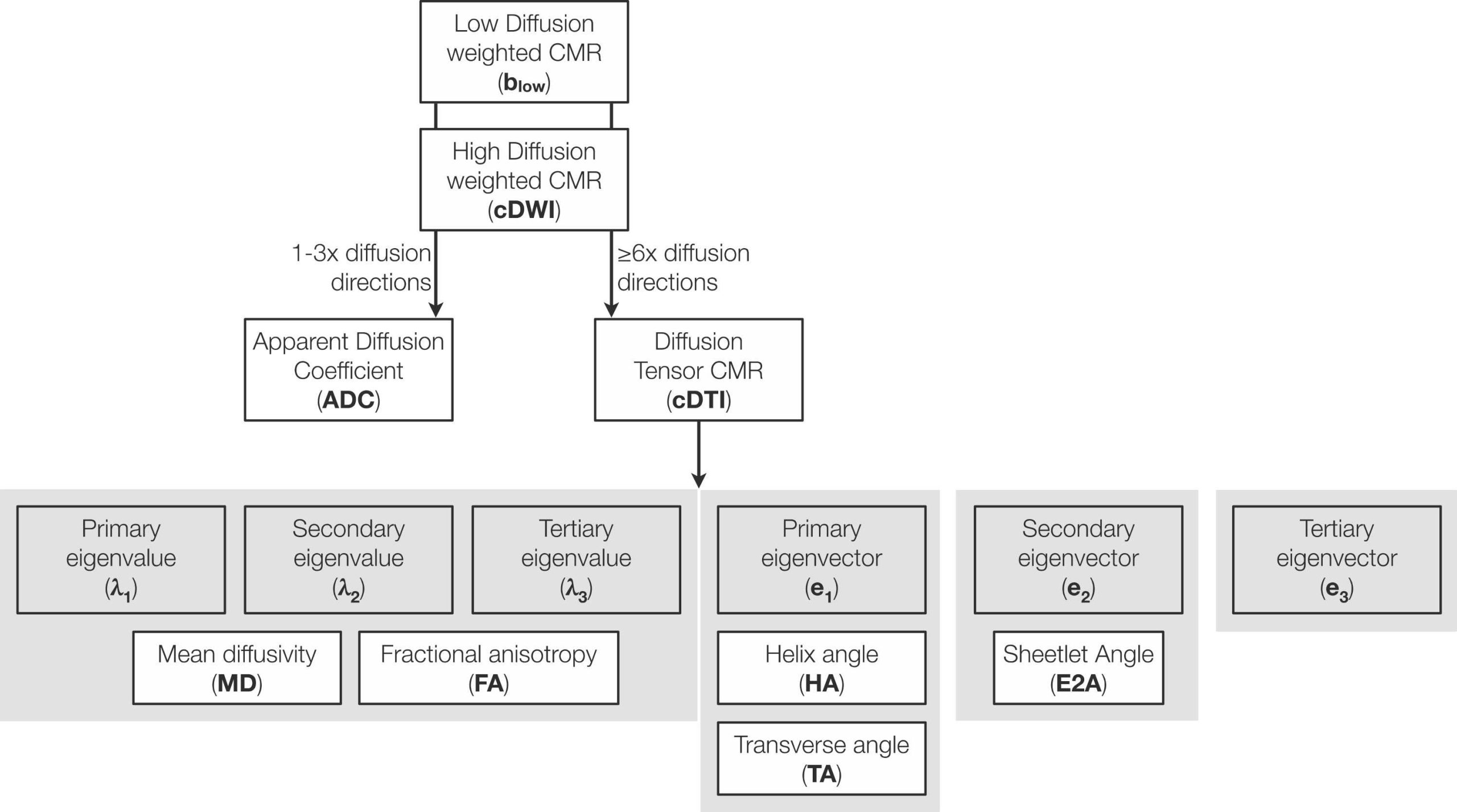
Fig.2 撮像~評価パラメータの取得までの概要(参考文献1.より引用)
HA、TA、E2Aの詳細は下記の通りです。1)

*HA、TA、E2Aは、局所心臓座標系(R,L,C)との間の角度から算出されます。(R:心臓の半径方向、L:長軸方向、C:周方向)
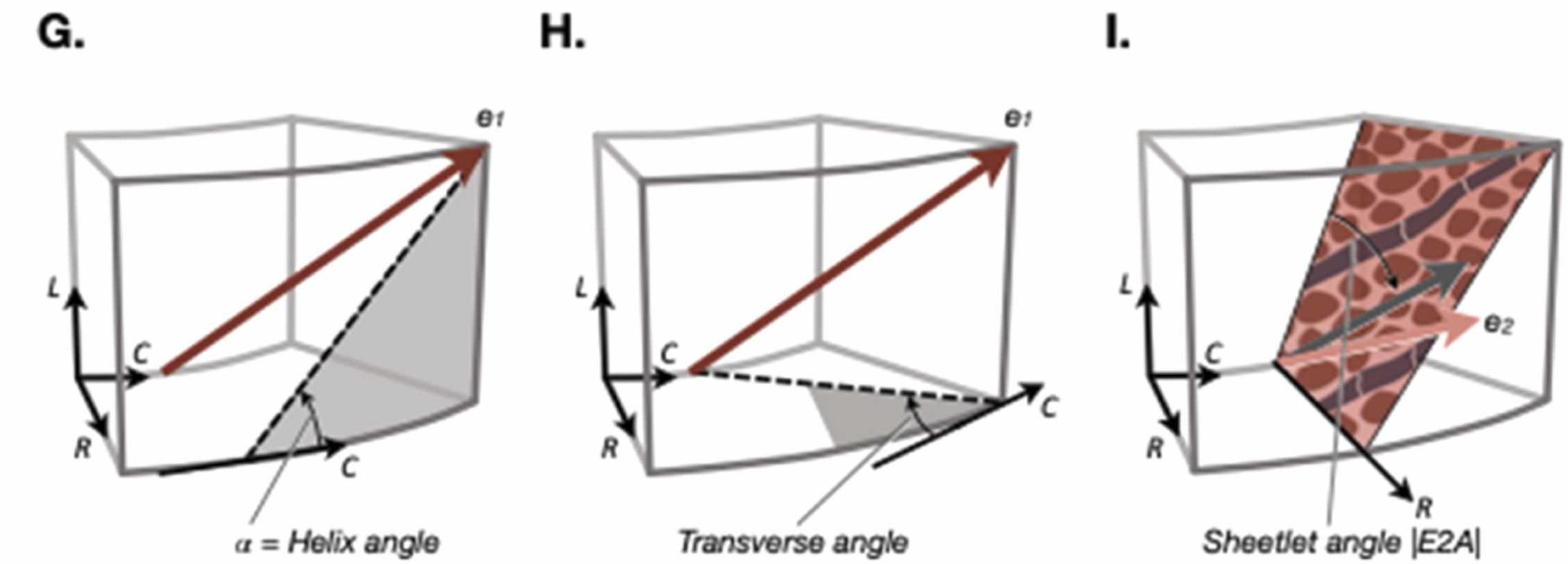
Fig.3 HA、TA、E2Aの概念(参考文献1.より引用)
cDTIでは、通常のDTI解析ツールで算出するFAやMDだけでなく、「局所心臓座標系」を使った定量値HA、TA、E2Aも対応可能なcDTI専用の解析ツールを利用します。
現時点で、cDTIを解析するための市販ソフトはありませんが、いくつかのオープンソースのツールが公開されております。
マイクロンは、国内の研究機関と専用ツールを利用したcDTI解析の方法論を構築しております。
3.cDTIと疾患
以下のような疾患でcDTIを利用した評価が報告されています。
◆肥大型心筋症(HCM)
HCM患者では、健常者に比較してFAの優位な低下がみられ、これらは心筋細胞配列の錯乱を反映していると考えられている。
従来のMRI検査結果(Cine、LGE)で、HCM患者の正常と判断された心筋セグメント部位(肥大がなく、線維化も認められない部位)においても、cDTIではFAや拡張期E2Aの指標に異常を認められている。これは肥大や線維化が顕在化する前の、早期の異常を捉えている可能性が高いと考えられている。8)
また、HCMの拡張期FAの低下は、NSVT(非持続性心室頻拍)の発生と独立して相関しており、突然死のリスク層別化に寄与する新たな指標として期待されている。6)
HCM患者は、収縮期E2Aが高く(過収縮)、本来角度が小さくなるはずの拡張期にもE2Aが大きい値を維持する状態(弛緩不全)にあり、健常者に比べE2Aの収縮期・拡張期の差であるE2A mobilityが著しく低下していることが報告されている。9)
◆急性心筋梗塞 (MI)
急性心筋梗塞では、FAが低下・MDが増加し、心筋細胞の錯乱や心筋細胞の喪失とそれに伴う細胞膜破裂を反映していることが考えられている。7)
MDとFAを用いることで、従来の遅延造影(LGE)を基準とした場合、90%以上の高い感度と特異度で急性梗塞の有無や範囲を特定できたと報告されている。腎機能障害を持つ患者において、造影剤を使用しない有力な診断ツールになることが期待されている。2)
急性期の梗塞部位における低いFA値や低い収縮期E2Aは、12か月後の左室悪性リモデリングの独立した予測因子となる可能性が報告されている。5)
その他、拡張型心筋症、心アミロイドーシス、大動脈弁狭窄症等の疾患でもcDTIを利用した報告が挙げられています。
4.おわりに
cDTIの分野は、撮像の難しさや市販の解析ソフトが無い等の要因により、依然として技術的に困難な課題を抱えています。それにもかかわらず、特に直近の数年間で注目を集めている評価手法であり、2025年にはSCMRからcDTIに関するconsensus1)も発表されております。またcDTIの標準化・ハーモナイゼーションを目的としたWG10)が発足するなど、臨床的実用化にむけて益々期待が広がっています。
参考文献
- Dall’Armellina E, Ennis DB, Axel L, et al. Cardiac diffusion-weighted and tensor imaging: A consensus statement from the special interest group of the Society for Cardiovascular Magnetic Resonance. J Cardiovasc Magn Reson. 2025;27(1):101109.
- Rajakulasingam R, Ferreira PF, Scott AD, et al. Characterization of dynamic changes in cardiac microstructure after reperfused ST-elevation myocardial infarction by biphasic diffusion tensor cardiovascular magnetic resonance. Eur Heart J. 2025;46(5):454-469.
- Joy G, Kelly CI, Webber M, et al. Microstructural and microvascular phenotype of sarcomere mutation carriers and overt hypertrophic cardiomyopathy. Circulation. 2023;148(10):808-818.
- Ashkir Z, Samat AHA, Ariga R, et al. Myocardial disarray and fibrosis across hypertrophic cardiomyopathy stages associate with ECG markers of arrhythmic risk. Eur Heart J Cardiovasc Imaging. 2025;26(2):218-228.
- Das A, Kelly C, Teh I, et al. Pathophysiology of LV remodeling following STEMI: A longitudinal diffusion tensor CMR study. JACC Cardiovasc Imaging. 2023;16(2):159-171.
- Ariga R, Tunnicliffe EM, Manohar SG, et al. Identification of myocardial disarray in patients with hypertrophic cardiomyopathy and ventricular arrhythmias. J Am Coll Cardiol. 2019;73(20):2493-2502
- Dall’Armellina E, Plein S. Diffusion tensor imaging to assess myocardial microstructure after infarction by magnetic resonance. Eur Heart J. 2025;46(5):470-472.
- Dong Z, Tang Y, Sun P, et al. Early identification of Myocardial microstructural alterations in Hypertrophic Cardiomyopathy with in vivo cardiac diffusion-Tensor Imaging. Radiol Cardiothorac Imaging. 2025;7(1):e240009.
- Ferreira PF, Kilner PJ, McGill LA, et al. In vivo cardiovascular magnetic resonance diffusion tensor imaging shows evidence of abnormal myocardial laminar orientations and mobility in hypertrophic cardiomyopathy. J Cardiovasc Magn Reson. 2014;16(1):87.
- Teh I, Moulin K, Ferreira PF, et al. Multi-center investigation of cardiac diffusion tensor imaging in healthy volunteers by the Society of Cardiovascular Magnetic Resonance Cardiac Diffusion Special Interest Group NETwork (SIGNET). J Cardiovasc Magn Reson. 2025;27(2):101948.
